カグリリンチドは、血糖値と食欲を調節する膵臓から分泌されるホルモンであるアミリンの作用を模倣する合成ペプチドです。38個のアミノ酸で構成されており、ジスルフィド結合を含んでいます。カグリリンチドは、脳、膵臓、骨などのさまざまな組織で発現される G タンパク質共役受容体であるアミリン受容体 (AMYR) とカルシトニン受容体 (CTR) の両方に結合します。これらの受容体を活性化することにより、カグリリンチドは食物摂取を減らし、血糖値を下げ、エネルギー消費を増加させることができます。カグリリンチドは、過剰な体脂肪と糖尿病、心血管疾患、および癌のリスク増加を特徴とする代謝障害である肥満の潜在的な治療法として研究されています。カグリリンチドは動物実験や臨床試験で有望な結果を示しており、2型糖尿病の有無にかかわらず肥満患者において大幅な体重減少と血糖コントロールの改善が実証されています。



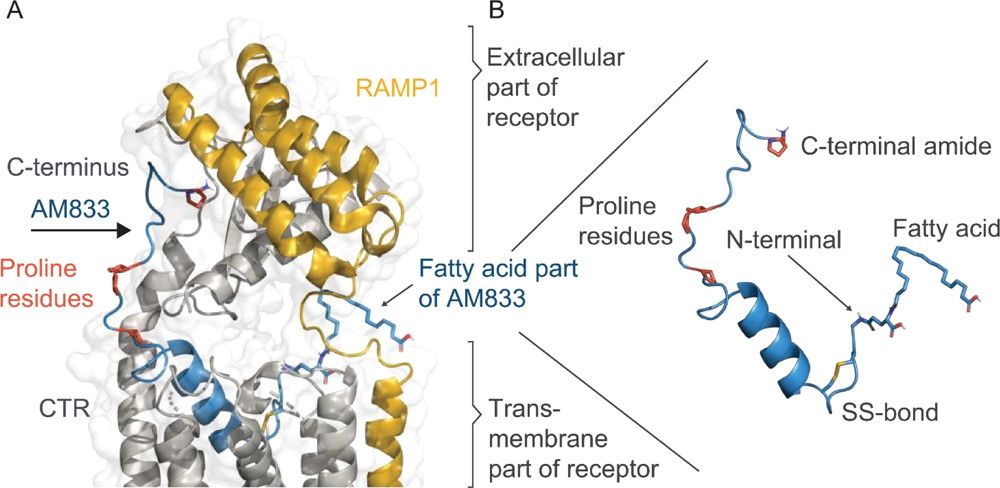
図 1. AMY3R に結合したカグリリンチド (23) の相同性モデル。(A) 23 の N 末端部分 (青) は、AMY3R の TM ドメインに深く埋め込まれた両親媒性αヘリックスによって形成されますが、C 末端部分は、23 の細胞外部分に結合する拡張された立体構造をとると予測されています。受容体。(29,30) 23 の N 末端に結合した脂肪酸、プロリン残基 (線維化を最小限に抑える)、および C 末端アミド (受容体結合に必須) が棒グラフで強調表示されています。AMY3R は、RAMP3 (受容体活性修飾タンパク質 3、オレンジ) に結合した CTR (灰色) によって形成されます。構造モデルは次のテンプレート構造を使用して作成されました: CGRP (カルシトニン受容体様受容体; pdb コード 6E3Y) の複合構造と 23 バックボーンのアポ結晶構造 (pdb コード 7BG0)。(B) 23 の拡大図。N 末端ジスルフィド結合、残基 14 と 17 の間の内部塩橋、「ロイシン ジッパー モチーフ」、および残基 4 と 11 の間の内部水素結合を強調しています。 (Kruse T、Hansen から改変) JL、Dahl K、Schäffer L、Sensfuss U、Poulsen C、Schlein M、Hansen AMK、Jeppesen CB、Dornonville de la Cour C、Clausen TR、Johansson E、Fulle S、Skyggebjerg RB、Raun K. カグリリンティド、ロングの開発-Acting Amylin Analogue. J Med Chem. 2021 Aug 12;64(15):11183-11194.)
カグリリンチドの生物学的用途には次のようなものがあります。
カグリリンチドは、食欲とエネルギーバランスを制御する脳領域である視床下部のニューロンの活動を調節することができます(Lutz et al., 2015, Front Endocrinol (Lausanne))。カグリリンチドは、空腹感を刺激する食欲抑制ニューロンの発火を抑制し、空腹を抑制する食欲抑制ニューロンを活性化します。たとえば、カグリリンチドは、2 つの強力な食欲誘発性ペプチドである神経ペプチド Y (NPY) とアグーチ関連ペプチド (AgRP) の発現を低下させ、プロオピオメラノコルチン (POMC) とコカインおよびアンフェタミン調節転写物 (CART) の発現を増加させることができます。視床下部の弓状核内の食欲不振誘発性ペプチド (Roth et al., 2018, Physiol Behav)。カグリリンチドは、体のエネルギー状態を知らせるホルモンであるレプチンの満腹効果も高めることができます。レプチンは脂肪組織によって分泌され、視床下部ニューロン上のレプチン受容体に結合し、食欲誘発性ニューロンを阻害し、食欲不振性ニューロンを活性化します。カグリリンチドは、レプチン受容体の感受性を高め、遺伝子発現に対するレプチンの効果を媒介する転写因子であるシグナルトランスデューサーおよび転写活性化因子3(STAT3)のレプチン誘発性活性化を増強することができる(Lutz et al., 2015, Front Endocrinol (Lausanne))。 。これらの影響により、食物摂取量が減り、エネルギー消費が増加し、体重減少につながります。
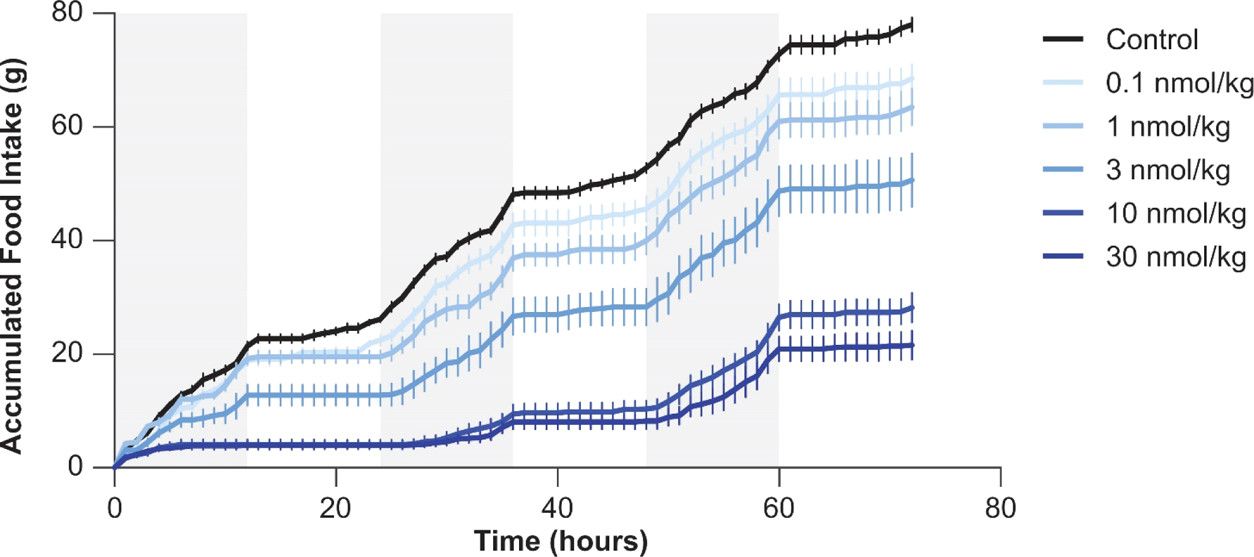
図 2. カグリリンチド 23 の皮下投与後のラットの食物摂取(Kruse T、Hansen JL、Dahl K、Schäffer L、Sensfuss U、Poulsen C、Schlein M、Hansen AMK、Jeppesen CB、Dornonville de la Cour C、 Clausen TR、Johansson E、Fulle S、Skyggebjerg RB、Raun K. 長時間作用型アミリン類似体であるカグリリンチドの開発. J Med Chem. 2021 Aug 12;64(15):11183-11194.)
カグリリンチドは、血糖値を制御する 2 つのホルモンであるインスリンとグルカゴンの分泌を調節します。カグリリンチドは、膵臓のアルファ細胞からのグルカゴン分泌を阻害し、肝臓による過剰なグルコース生成を防ぎます。グルカゴンは、肝臓でのグリコーゲンの分解とグルコースの合成を刺激し、血糖値を上昇させるホルモンです。カグリリンチドは、環状アデノシン一リン酸(cAMP)レベルとカルシウム流入を低下させる抑制性Gタンパク質に結合しているアルファ細胞上のアミリン受容体とカルシトニン受容体に結合することにより、グルカゴン分泌を抑制することができます。カグリリンチドは、膵臓のベータ細胞からのインスリン分泌を増強し、筋肉や脂肪組織によるグルコースの取り込みを促進します。インスリンは、肝臓や筋肉でのグルコースのグリコーゲンとしての貯蔵と、脂肪組織でのグルコースの脂肪酸への変換を促進し、血糖値を低下させるホルモンです。カグリリンチドは、cAMP レベルとカルシウム流入を増加させる刺激性 G タンパク質と結合しているベータ細胞上のアミリン受容体とカルシトニン受容体に結合することにより、インスリン分泌を促進します。これらの効果は血糖値を低下させ、インスリン感受性を改善することができ、2型糖尿病を予防または治療することができます(Kruse et al., 2021, J Med Chem; Dehestani et al., 2021, J Obes Metab Syndr.)。
カグリリンチドは、骨の形成と吸収に関与する 2 種類の細胞である骨芽細胞と破骨細胞の機能にも影響を与える可能性があります。骨芽細胞は新しい骨基質を生成する役割を果たし、破骨細胞は古い骨基質を破壊する役割を担います。骨芽細胞と破骨細胞のバランスによって、骨の量と強度が決まります。カグリリンチドは骨芽細胞の分化と活性を刺激し、骨形成を増加させます。カグリリンチドは、骨芽細胞上のアミリン受容体およびカルシトニン受容体に結合することができ、これにより、骨芽細胞の増殖、生存、および基質合成を促進する細胞内シグナル伝達経路が活性化される(Cornish et al., 1996, Biochem Biophys Res Commun.)。カグリリンチドは、骨芽細胞の成熟および機能のマーカーであるオステオカルシンの発現も増加させることができる(Cornish et al., 1996, Biochem Biophys Res Commun.)。カグリリンチドは破骨細胞の分化と活性を阻害することもでき、これにより骨吸収が減少します。カグリリンチドは、破骨細胞前駆体上のアミリン受容体およびカルシトニン受容体に結合することができ、これにより成熟破骨細胞への融合が阻害されます(Cornish et al., 2015)。カグリリンチドは、破骨細胞活性および骨吸収のマーカーである酒石酸耐性酸性ホスファターゼ(TRAP)の発現も低下させることができます(Cornish et al., 2015, Bonekey Rep.)。これらの効果は、骨密度を改善し、骨量の低下と骨折リスクの増加を特徴とする状態である骨粗鬆症を予防または治療することができます(Kruse et al., 2021; Dehestani et al., 2021, J Obes Metab Syndr.)。







